1. 바이오의약품의 비경구적 투여
○ 비경구적 투여(Parenteral administration)의 종류와 목적: 바이오의약품은 경구를 통한 비흡수 및 표적기관에로의 직접적인 투여를 위해 비경구적 투여(Parenteral administration)이며 대표적으로 주사(injection) 방법이다. 주사 (injection) 란 시험물질 투여의 일종으로 주사기를 이용하여 비경구적으로 체내 투여하는 방법이다. <그림>은 랫드에 대한 다양한 주사방법인데 물질을 주사기에 넣어 주사하는 부위에 따라 방법이 다르다. 척수내 주사 (intrathecal injection) , 뇌실질내 주사 (intracerabral injection) , 동맥내 주사 (intra-arterial injection) , 국소도포 (topical application) , 역안와 주사 (retro-orbital injection) , 기도와 폐에 도달하는 비강내 점적노출( nasal instillation) 과 분무 (nebulization) . 복강내 조사 (intraperitoneal injection) , 간문맥 주사 (intraporteal injection) , 종양내 주사 (intratumoral injection) , 방광내 주사 (intravesical injection) , 미정맥 주사 (tail vein injection) 등 을 주사방법의 예로 들 수 있다. 주사를 통한 물질의 주입은 크게 3가지 목적으로 이루어진다. 첫 번째 목적은 전신혈관계 내에서 시험물질의 용량을 높이기 위함이다. 예를 들어 경구투여를 통해서는 간에 의한 초회통관대사로 전신혈관계로 들어가는 용량이 많이 감소하게 된다. 두 번째 목적은 기관 보호를 위해 시험물질의 출입을 막는 장벽(barrier)을 극복하기 위한 것이다. 예를 들어 뇌에는 혈액-뇌 장벽 (blood-brain barrier) 이 존재하여 치료에 효능이 있는 약물이 뇌 또는 척수에 도달하는 경로를 막는다. 이러한 경우에 시험물질 또는 약물 주입을 위하여 뇌척수강 내 주사방법이 응용된다. 세 번째 목적은 약물 등의 시험물질이 표적기관 이외로의 유입을 최소화하기 위함이다. 항암제는 독성이 상당히 강하여 종양이 발생한 부위에만 주 입된다. 이는 항암제가 다 른 부위로의 이동을 최소화하여 독성을 예방하기 위함이다.
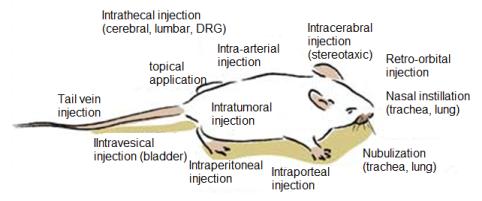
<그림> 다양한 주사(injection) 방법: 랫드에 대한 다양한 주사방법인데 물질을 주사기에 넣어 주사하는 부위에 따라 다양한 방법이 있는데 척수내 주사(intrathecal injection), 뇌실질내 주사(intracerabral injection), 동맥내 주사 (intra-arterial injection), 국소도포(topical application), 역안와 주사(Retro-orbital injection), 기도와 폐에 도달하는 비강내 점적노출(nasal instillation)와 분무(nebulization). 복강내 조사(intraperitoneal injection), 간문맥 주사(intraporteal injection), 종양내 주사(intratumoral injection), 방광내 주사(intravesical injection), 미정맥 주사(tail vein injection) 등을 예로 들 수 있다. DRG: Dorsal Rool Ganglia, 등배신경절.
2. 바이오의약품의 비경구적 주사에 의한 독성학적 문제점
○ 비경구적 투여로의 문제점과 더불어 다음과 같이 바이오의약품의 본질적 문제 및 물리적 문제에 의한 3가지 독성학적 특징을 가지고 있다.
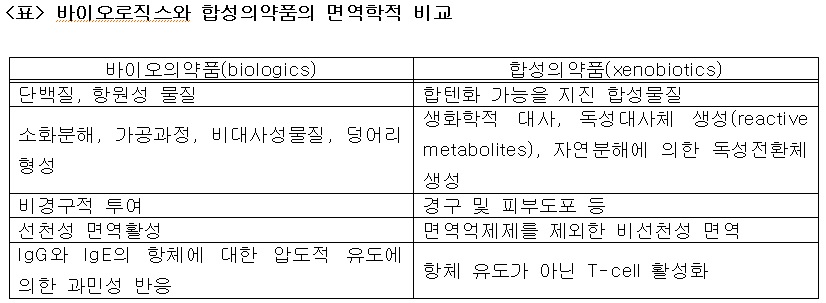
① 알레르기 과민성 반응: 대부분의 바이오의약품은 큰 분자량으로 인하여 잠재적으로 알레르기 과민성 반응(allergic hypersensitivity reactions) 을 유도할 수 있다. 아래의 <표>는 바이오의약품(biologics)과 합성의약품(xenobiotics)의 면역학적 측면에서 차이점을 제시한 것이다. 이이과 관련하여 <켐온 칼럼> Biologics의 약물학적 및 독성시험학적 측면에 대한 이해-(1)의 TGN1412 사건이 대표적인 예이다.
② 감염병의 위험성: 류마티스 관절염(Rheumatoid Arthritis), 건선(Psoriasis) 그리고 다른 면역-관련 질환을 치료하기 위한 바이오의약품은 면역체계 활성 저하를 유도하여 감염병의 위험성을 증가를 유도할 수 있다.
○ 투여시 1차 감염: 때론 바이오의약품이 인체 면역반응 활성을 저해할 경우에는 과잉 반응의 알레르기 반응 등의 치료에 도움이 된다. 그러나 합성의약품에 의한 경우에 다르게 바이오의약품 투약은 표적 투약으로 감염의 위험이 있어 이러한 경우에는 면역반응을 억제하는 바이오의약품인 경우에는 감염병에 더욱 취약함을 나타낸다. 따라서 바이오의약품 투약시 합성의약품보다 감염병에 더욱 취약하다는 것이 일반적인 견해이다. 연구에 따르면 바이오의약품의 투약시 환자의 2-5% 정도에서 심각한 감염의 우려 가 있는 것으로 추정되고 있다. 감염은 신체의 여러 부위에서 발생하지만 상기도 감염(Upper respiratory infections)이 되는 특성이 있다. 따라서 면역억제제의 합성의약품과의 병용 투여는 바이오의약품에 의한 감염에 대한 위험성을 더욱 높이게 된다.
○ 감염의 재활성(Infection reactivation): 감염의 재활성은 hepatitis B virus를 보유는 하지만 활성이 없는 환자에게 발생의 예를 들 수 있다. 이러한 사람에게 바이오의약품의 투여는 기존의 비활성화된 hepatitis B virus의 활성 및 간독성을 유도할 수 있다. 결핵(tuberculosis)도 유사한 과정으로 바이오의약품에 의해 활성화 될 수 있다. 비활성 결핵균(tuberculosis bacteria)을 보유한 환자에게 바이오의약품을 투여한 경우에는 균이 활성화되어 호흡에 문제를 유발할 수 있다. 따라서 바이오의약품 투여시에는 항상 특정균에 대한 모니터링이 우선적으로 필요하고 활성화에 대한 영향을 확인할 필요성이 있다.
③ 바이오의약품의 주입부위 반응(injection site reactions, ISR) : 바이오의약품은 표적기관에 직접적으로 주입되는 경우가 많이 투약과 관련된 부작용(infusion-related reactions)인 주입부위 반응(injection site reactions, ISR), 그리고 정맥투입을 통해 주입 반응(infusion reaction)을 유도할 수 있다, 이는 바이오의약품의 표적기관 투여에 의한 대표적인 반응이다. 실제적으로 대부분의 CRO 기관에서 뇌실내 주사(intracerebroventricular injection, ICV), 척수내 주사 (intrathecal injection) , 뇌실질내 주사 (intracerabral ventrical injection)와 뇌내주사(intra에 대한 주사 미숙으로 유효성 및 독성에 대한 올바른 자료 획득 및 이에 의한 해석이 어려움이 있는 것이 사실이다, 바이오의약품 비임상시험에 대한 이러한 문제를 해결하고 극복하기 위해 (주)켐온은 최첨단 장비 계획과 수많은 연습으로 최선을 하고 있다.
4. 바이오의약품의 주입부위 반응(injection site reactions, ISR)
1) ISR의 개념
○ 바이오의약품은 치료를 위해 매우 정확한 표적-특이적(target-specific) 특성을 가지고 있다. 즉, 합성의약품과 같이 경구 또는 주사 등 비수술적 투약이 대부분이지만 바이오의약품인 경우에는 표적-특이성에 기인하여 질병과 관련 조직 및 기관에 외과적 수술을 통한 주입과 주사에 의한 주입 특성을 가지고 있다. 이에 바이오의약품의 특정 기관에 주입되는 부분에서만 발생하는 독성인 국소독성(local toxicity)의 원인이 되며 이를 주입 부위반응(injection site reaction, ISR)이라고 한다. 이는 합성의약품이 전신혈관계로 들어가 표적기관에 이외의 장소에서 발생하는 전신독성(systemic toxicity)과 차이점이라고 할 수 있다, 특히 합성의약품이 혈장에서 PK 시험을 통해 약물의 복용 특성을 파악하지만 바이오의약품인 경우에는 표적기관에서 벗으나 다른 조직으로 이동(biodistribution) 및 표적기관에서 지속성(persistence)이 독성에 대한 이해와 처방전을 결정하는 중요한 파라미터가 된다. 인체에 있어서 바이오의약품의 주사를 통해 가장 흔히 발생하는 ISR 으로 Burning or stinging, Red rash, Itching, Swelling, Bruising, Soreness 등의 증상들이 나타날 수 있다, 물론 이러한 증상들이 동물과 동일하게 나타나지는 않지만 주입 방법의 정확성 및 정교함의 차이로 동물실험에서 더 심각한 ISR 이 발생할 수 있다, 따라서 ISR 은 동물실험에서 주사 및 외과적 수술을 통한 주입의 미숙으로 발생할 수도 있어 동물을 이용한 독성시험 및 유효성시험에서 바이오의약품의 주입은 치료에 영향을 미치는 아주 중요한 기술적 요인이라고 할 수 있다.
2) ISR의 발생율의 예시
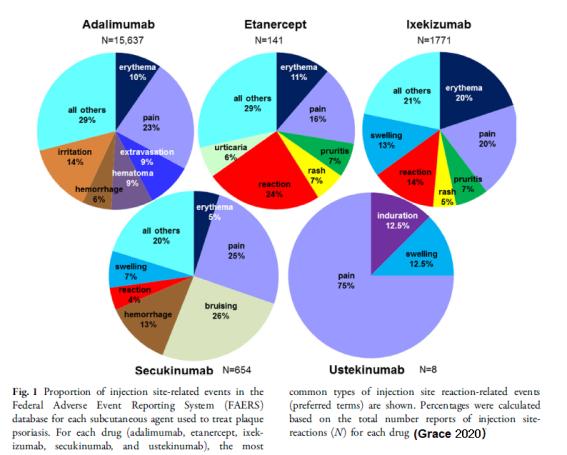
○ 바이오의약품의 피하주사(subcutaneous injection): 바이오의약품의 피하주사일때 ISR이 가장 빈번히 발생하는데 경에 따라서는 ISR이 IgE-매개 면역반응(IgE-Mediated Reactions) 또는 비 IgE-매개 면역반응인 T세포 매개 면역반응(T cell-mediated reactions)을 유도한다. Fig. 1은 중증의 판상형 건선(severe plaque psoriasis) 치료를 위해 사용된 바이오의약품인 adalimumab, etanercept, ixekizumab, secukinumab, 그리고 ustekinumab 등을 USFDA 허가 후 2년 동안 피하주사하였을 때 발생한 ISR-관련 보고 내용이다. 승인받은 의약품의 부작용을 보고하는 US FDA의 FAERs 데이터베이스에 따르면 adalimumab의 15637, etanercept의 141, ixekizumab의 1771, secukinumab의 654 그리고 ustekinumab의 8건 보고가 이루어졌다. Fig 1에서는 개별 바이오의약품의 보고 ISR 건수에 대한 특정 증상을 비율로 나타낸 것이다. 가장 빈번히 발생하는 증상은 주사부위(injection site)의 통증(pain)으로 전체 ISR 중 23% (adalimumab), 16% (etanercept), 20% (ixekizumab), 25% (secukinumab), 그리고 75% (ustekinumab) 등으로 확인되었다(Elsie Grace et. al., Dermatol Ther (Heidelb) 2020; 10:99 106). 각 약물에서 확인된 ISR의 증상별 비율은 adalimumab에 대해서는 pain (통증, 23.3%), irritation (자극성, 14.1%), 그리고 erythema (홍반, 9.6%), etanercept에 대해서는 reaction (반응성, 24.1%), pain (16.3%), 그리고 erythema (11.4%), ixekizumab에 대해서는 erythema(19.9%), pain (19.8%), 그리고 reaction (13.6%) secukinumab에 대해서는 bruising (타박상, 25.7%), pain (25.4%), 그리고 hemorrhage (출혈, 12.5%), ustekinumabdp 대해서는 pain (75%), induration (경화, 12.5%), 그리고 swelling (부기, 12.5%)으로 확인되었다.
5. 뇌와 관련된 주사
1) 종류
○ 바이오의약품의 뇌와 관련 3대 주사 부위: 뇌 조직에 직접 주사하는 뇌내주사 (intracerebral injection), 뇌실(cerebral ventricle)에 주사하는 뇌실내 주사(intracerebroventricular injection, ICV), 척수강내 주사 (intrathecal injection) , 등이 대표적인 뇌와 관련된 바이오의약품의 주사 방법이다. 바이오의약품은 합성의약품보다 수백배 크기 때문에 체내에 흡수되어 뇌실 또는 뇌조직으로 이동하려면 BBB(blood brain barrier)를 통과가 어렵다. 이러한 이유로 뇌의 표적 위치에 직접 주입을 위해 뇌내주사(intracerebral injection)와 뇌실내 주사(intracerebroventricular injection, ICV) 기법이 응용된다.
2) 뇌내주사(intracerebral injection)와 stereotaxic apparatus
○ 뇌내주사(intracerebral injection) 장비: 뇌내주사는 뇌조직 자체가 injection site이 된다. 뇌 조직 자체에 injection은 injection volume이 크면 그에 따른 부작용이 크다. 따라서 마우스 및 랫드에 대한 적절한 바이오의약품의 주입 액량이 요구된다. 이를 위해 <그림>처럼 stereotaxic apparatus(소동물용뇌심부고정장치) 를 사용하는 것이 중요하다(Mathon et. al. 2015). Stereotaxic apparatus(소동물용 뇌심부 고정장치): Stereotaxic surgery이란 소동물용 뇌심부 고정장치를 사용하여 살아있는 설치류 등의 소동물의 뇌의 수술적 조작을 의미한다. 소동물의 뇌수술에 대부분은 Stereotaxic apparatus가 응용될 정도로 상당히 유용한 장치이다. 소동물의 뇌수술시에 깊이 있는 뇌의 표적위치를 시각적으로 보는 것이 불가능하여 정확하게 수술 또는 주사하는데 상당히 어렵다. Stereotaxic apparatus는 <그림>과 같이 시각적 경계표지에 대한 뇌의 공간적 관계와 연결되어 있어 표적위치를 명확하게 구별할 수 있도록 개발 되었다.
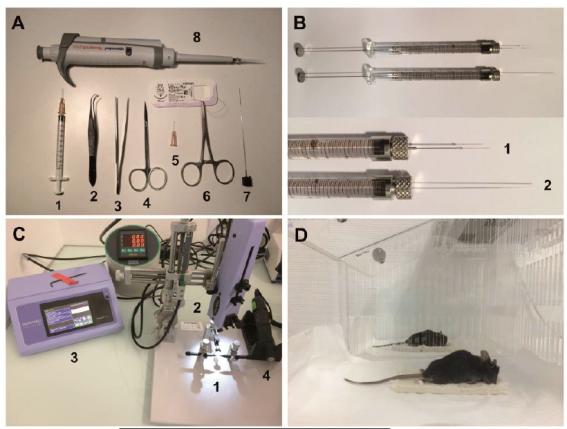
<그림> 마우스의 뇌내주사를 위한 장비. (A) Surgical tools. 1, 1ml syringe for anesthesia; 2 and 3, fine forceps; 4, surgical scissors; 5, surgical hook; 6, needle holder with surgical braided absorbable suture; 7, black leader for human spinal anesthesia; 8, 10 μl calibrated micropipette. (B) 10 μl injection syringes with 1, flexible or 2, rigid 33 gauge needle. (C) Surgical area. 1 and 2, Stereotaxic apparatus with stereotaxic atlas; 3, Stereotaxic injection system; 4, High speed dental drill with small drill bits. (D) Temperature-controlled heating cage(Mathon et. al. 2015).
○ 일반적으로 뇌내주사는 아래의 <그림>과 Ear line과 Eye line과 정수리(bregma) 선의 교차지점에 위치한다.
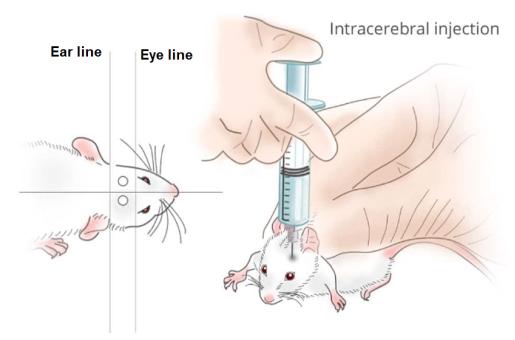
<그림> 뇌내주사의 개략적 위치
○ 마우스의 Craniotomy(개두술)과 the dura(뇌경막) 오픈과 주입: 두개내에서의 수술적 처치를 하기 위해 두개를 여는 조작을 개두술이라고 하며 다음과 같은 순서 및 <그림>과 같이 주입이 이루어진다.
① Use a dissecting microscope at ×20 to ×40 magnification. Consider the position of bregma (정수리, 두개골을 이루고 있는 여러 개의 뼈들이 만나는 면에 형성되는 관상 봉합선과 시상 봉합선의 교차 부위. 뇌의 입체 정위 수술시 기준점) as the reference (stereotaxic zero) of the X and Y coordinates
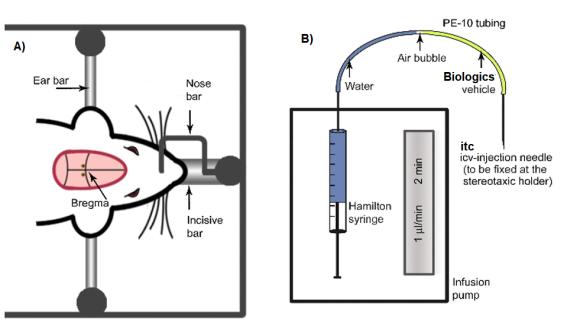
<그림> Stereotexic apparatus에서의 bremgma(정수리) 위치와 뇌내주사(itc) 및 뇌실내주사(icv)의 장치(B)
② Using predefined stereotaxic coordinates, mark on the skull the intended site of injection. Adjust the drill to 20,000 rpm
③ Using a 26-gauge surgical hook, remove the small pieces of any remaining skull to expose the dura.
④ Finally, position the syringe over the craniotomy and check that the it is not diverted by the edge of the burr-hole.
⑤ Adjust the features of fluid aspiration on the injection system (the aspirated volume should be 10% larger than the injected volume , or at least +100 nl for small volumes). Aspiration speed can be up to 38 μl/min (slower aspiration is preferred for viscous fluid). Make sure that the needle is not clogged by ejecting a small volume of fluid (e.g. 50 nl) under visual control.
⑥ Lower the syringe needle to the desired depth ( Z coordinate of the injection site) in the brain parenchyma(뇌실질: 신경세포와 아교세포로 구성되어 뇌의 기능성조직) (Fig. 2G).
⑦ Adjust the features of fluid injection on the injection system. The injection of the fluid should be very slow to avoid an acute increase of intracranial pressure and facilitate diffusion of the fluid (rate of injection should not be >100 nl/min) .
⑧ Depending on the total volume injected, this step may take up to 10 min. We limit the maximal injection volume to no more than 1500 nl in one session.
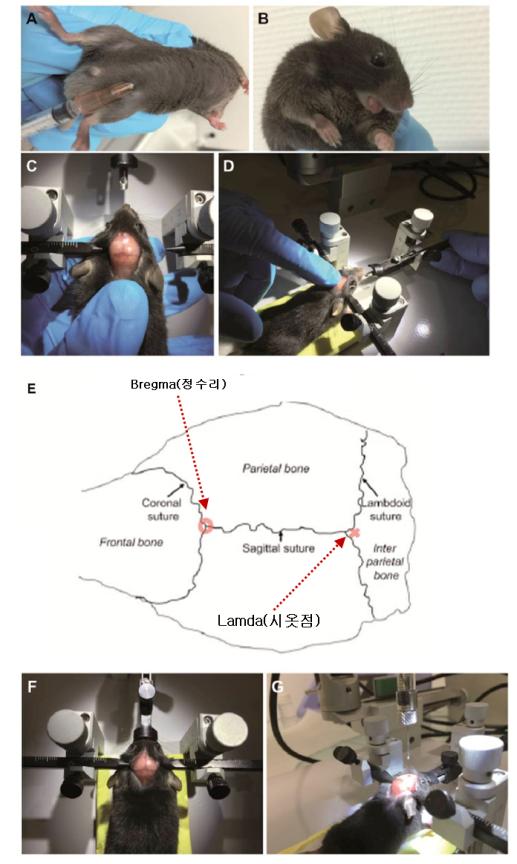
<그림> Procedure of stereotaxic intracerebral injection in adult mice. (A) The ketaminexylazine mixture is injected intraperitoneally through a 21-gauge needle inserted into the lower right abdominal quadrant. (B) The tongue of the mouse is pulled out to facilitate breathing. Lubricant ophthalmic gel is applied on both eyes to avoid keratitis during surgery. (C) The head of the mouse is held in place to allow positioning of the right ear bar. (D) The head of the mouse is moved up to insert the incisor adapter. (E) Stereotaxic landmarks on the skull of the mouse. Bregma is represented by the red circle and lambda by the red cross. (F) The snout clamp is placed just below the eyes. Before beginning injection, the skull is perfectly flat. (G) The syringe needle is lowered through the craniotomy to the desired depth; then the injection is started.
⑨ 바이오의약품의 stereotaxic intracerebral injection의 정확도 결과: 성체 마우스에서 표적기관인 <그림>에서처럼 시상의 전등쪽핵(the anterodorsal nucleus of the thalamus, ADN)에 270번을 주사하여 249번의 형광물질이 ADN에 나타나는 효율성이 확인되었다.
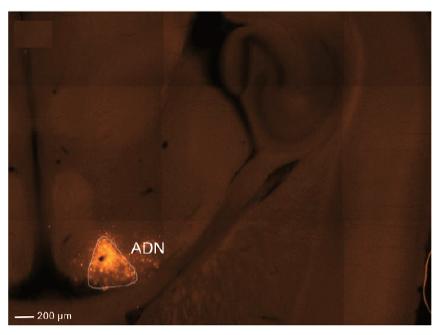
<그림> 4. Accuracy of injection sites: Horizontal slice (DV = -2.85 mm). Stereotaxic injection of m-cherry expressing anterograde(기억상실) glycoprotein-deleted rabies virus (RABV ΔG (VSV GRtmC); 300 nl) in the anterodorsal nucleus of the thalamus(ADN, 시상의 전등쪽핵) in an adult mouse (P28). The animal was sacrificed at P36.
3) 뇌실내 주사(intracerebroventricular injection, ICV)와 stereotaxic apparatus
○ 뇌실내주사가 뇌내주사와의 차이 는 바이오의약품의 주사 부피에 있다. 뇌내주사는 뇌조직 자체에 주입됨으로 공간이 작아 injection volume이 크면 그에 따른 부작용이 매우 클 수 밖에 없다. 대략적으로 랫드의 경우에 1μl 이하의 부피만 가능하다. 반면에 뇌에는 연결된 빈 공간을 가지고 있는데, 이러한 부분들이 서로 연결된 빈 공간을 뇌실(cerebral ventricle)이라고 한다. 마우스의 경우에는 뇌의 size가 rat에 비해서 작아 정확한 injection이 쉽지가 않다, 그러나 마우스의 뇌실 즉 ventricle에 주사를 할 경우는 상당히 넓은 부위가 injection site가 되므로 더 용이할 수 있다. 뇌실 외에 아주 특정한 뇌의 위치에만 주사한다면 Intracerebral injection이 이루어져야 한다, 반면에 ICV는 혈액 뇌 장벽(blood brain barrier, BBB)을 우회하기 위해 뇌실에서 뇌척수액으로 직접 물질을 침습적으로 주입하는 기술이다. BBB는 뇌를 효과적으로 보호하지만 중요한 약물이 중추신경계(CNS, central nervous system)에 들어가는 것을 막을 수 있다. 합성의약품의 주입을 위해서도 ICV 기술이 응용되지만 CNS-관련 마우스 질환모델에 therapeutic RNAs, plasmid DNA, 그리고 viral vector 등의 바이오의약품을 뇌실에 주입할 때 사용되는 방법이다, 인체의 경우에는 신경퇴행성 질환(neurodegenerative disorders)인 척수근육위축(spinal muscular atrophy, SMA), 또는 신경교종(gliomas)의 치료제 투여, 그리고 CNS에 신경영양인자(neurotrophic factors) 전달을 위해 응용되는 주입 기술이다.