○ 이전 칼럼의 아토피피부염에 대한 요약
○ 아토피피부염은 1970년대까지는 6세 이하 소아에서 약 3%의 발생에 불과하였지만 최근에는 소아 20%, 성인에서도 1~3% 정도로 발생하는 추세로 지난 30년 동안 증가하고 있다.
○ 아토피 및 아토피피부염의 유발과 관련된 유전자는 약 30 여개 유전자가 확인되었다.
○ 아토피피부염을 가진 환자 특히 어린이 환자는 정신적 스트레스가 크며 이는 궁극적으로 호르몬 변화를 유도하여 아토피피부염을 악화시킬 수 있다.
○ 면역학적 측면에서 아토피피부염의 특성은 선천성면역의 약화되며 후천성면역의 Th1 및 Th2세포 불균형으로 정의할 수 있다.
○ 아토피피부염 발생 및 진행의 시기와 병변의 특징에 따라 발병기(onset), 급성병기(acute phase) 그리고 만성병기(chronic phase)로 구분되어 설명되는데 각 병기에서 각각의 다른 T-세포 활성 변화가 중요한 역할을 한다.
○ 아토피피부염에서 활성화된 비만세포는 다양한 매개체 및 사이토카인을 분비하여 Th2세포-지배적인 활성(Th2 skewing), 피부염증반응(skin inflammation)과 소양증(pruritus)을 유발한다.
○ 아토피피부염은 외인성 과 내인성 아토피피부염으로 구분되며 IgE 혈청농도의 변화에 따라 구분된다.
○ 선천선 피부장벽의 장애는 외인성 아토피피부염 유발에 있어서 결정적인 역할을 한다.
○ 아토피피부염에서 가려움은 피부의 표피와 진피에 독보적으로 분포되어 있는 C-신경체(C-neuron) 또는 C-민말이집섬유(unmyelinated C-fibers)를 통해 중추신경계로 전달된다.
○ 아토피 행진이란 장기간에 걸쳐 아토피피부염이 알레르기 비염, 천식으로 전환되는 과정을 의미한다.
○ 아토피피부염의 랑게르한스세포의 IgE-고친화성 수용체 단백질(FcεRI) 발현은 천식과 알레르기 비염의 중증도와 밀접한 관계가 있으며 이는 아토피 행진을 유도하는 주요 기전으로 이해된다.
1. 항아토피피부염 약물 개발을 위한 동물모델의 종류
○ 아토피피부염의 동물모델은 1997년 NC/Nga 마우스로부터 아토피피부염-유사 피부병변이 제시된 후 다양하게 개발되어왔다. 일반적으로 아토피피부염 모델을 위한 동물은 주로 마우스가 이용되는데 다음과 같은 2가지 모델인 ① 자연발생적으로 피부병변이 발생하는 자연발생모델, ② 단일 또는 복합 알러젠의 피내 투여에 의한 감작(sensitization, 일차 면역반응을 유발하거나 과민성반응을 유도하기 위한 알러젠 또는 항원 투여)과 야기(challenge, 감작된 동물에 동일한 항원을 재투여하여 면역세포의 기억기능에 의해 유발되는 면역반응)의 hapten-유발 모델이 널리 이용되고 있다. 이 외에도 Tape-stripping/epicutaneous OVA sensitization, 집먼지 진드기-페치 모델, 유전자의 형질전환 및 유전자 제거의 유전자 조절을 통한 아토피피부염 모델이 있다.
2. 자연발생 모델
1) 개념 및 특성
○ 아토피피부염의 자연발생 모델로는 NC/Nga 마우스가 이용된다. NC/Nga 마우스를 특정 균-부재 (specific-pathogen free, SPF) 사육실이 아닌 일반 환경과 같은 사육실에서 사육하면서 자연적으로 아토피피부염-유사 병변이 발생하는 원리를 이용한 것이다. 자연발생 모델에 의한 아토피피부염의 면역학적 변화는 Th2세포에 분비되는 사이토카인과 케모킨 증가, IL-4에 의한 B-세포 활성으로 혈청 IgE 농도 증가, 호산구 침윤 등이 있으며 이는 사람에서의 아토피피부염의 면역학적 변화와 유사하다. 또한 홍반을 비롯한 부종, 출혈, 가피와 피부건조 등의 아토피피부염의 임상적 병변도 NC/Nga 마우스에 유발되며 사람과 유사한 측면이 있다. 사람에 있어서 아토피피부염의 병변이 출생 후 8주부터 나타나기 시작하여 17주에 최고의 중증도가 나타난다. NC/Nga 마우스에서도 8주부터 IgE 혈청농도가 증가하여 피부병변의 중증도가 17주에 최고조에 달한다. <표-1>은 NC/Nga 마우스를 이용한 지연발생 모델에 대한 특성을 나타낸 것이다.

2) 단점
○ 그러나 NC/Nga 마우스에 유도된 아토피피부염-유사 병변이 전형적인 특성인 Th2세포 활성과 IgE 증가와 무관하게 발생한다는 단점이 있다. 이러한 단점은 NC/Nga 마우스에서 Stat6 유전자를 제거한 모델에서 확인할 수 있다. Stat6 단백질은 Th2세포의 분화 촉진뿐 아니라 IL-4-매개 면역반응을 유도하는 신호전달물질이다. IL-4는 Th2세포에서 분비되어 B-세포를 자극하여 IgE 분비를 촉진시킨다. NC/Nga 마우스에 stat6 유전자를 제거하여 사육을 하게 되면 Th2세포 활성과 IgE 혈청농도가 감소하여 피부병변도 사라지게 되는 현상을 기대할 수 있다. 그러나 NC/Nga 마우스에 stat6 유전자를 제거한 후 관찰한 결과, 피부병변은 사라지지 않고 오히려 Th1세포의 활성 증가와 더불어 Th1세포-유래 사이토카인인 IFN-γ가 증가하였다. 이는 NC/Nga 마우스에서 유도된 아토피피부염-유사 피부병변이 Th2세포-비의존성 및 IgE-비의존성으로 발생할 수 있다는 것을 의미한다. 따라서 NC/Nga 마우스의 자연발생 모델을 이용한 치료 약물 개발을 위해 아토피피부염 표적기전에 대한 충분한 이해와 더불어 접근이 필요하다.
3) 일반 환경 및 SPF 환경의 차이점
○ SPF 환경이 아닌 일반 환경에서 진드기를 투입하면 NC/Nga 마우스에서 아토피피부염이 유발되며 ivermectin을 살포하여 진드기를 퇴치하면 IgE 농도가 감소될 뿐 아니라 병변도 사라진다. 일반적으로 비-SPF 시설에서 NC/Nga 마우스의 아토피피부염 발생률은 약 50% 정도이다. 그러나 SPF 시설에서 NC/Nga 마우스 사육을 통한 아토피피부염의 발생률은 시설에 따라 큰 차이가 나지만 대략적 5%이하이다. SPF 시설에서 낮은 발생률을 극복하기 위해서는 NC/Nga 또는 C57BL/6의 피부에 진드기추출물 또는 황색포도상구균( Staphylococcal aureus )에서 분비되는 enterotoxin B의 도포가 필요하다. 대부분 이들 유도물질에 의해 습진성 병변이 유발되는데 표피의 손상이 더욱 악화된 미란성 병변 유도를 위해서는 우두 바이러스(vaccinia virus) 감염을 하기도 한다. 또한 단일물질의 hapten을 도포하기도 한다. 이와 같이 자연발생 모델은 외부 환경의 공기가 이동이 가능한 사육실( air-uncontrolled conventional room)에서 자연발생적으로 아토피피부염-유사 피부염을 유도하는 모델이며 NC/Nga 마우스를 이용한 모델이다.
4) 자연발생 모델의 사례
○ <그림-1>은 ICR 마우스와 NC/Nga 마우스를 일반 환경에서 약 10주 동안의 자연발생모델을 통해 확인된 육안적 관찰과 조직병리의 현미경 관찰을 나타낸 것이다. <그림-1>의 A)에서처럼 ICR 마우스인 경우에는 어떠한 병변도 없었다. 반면에 <그림-2>의 B)에서처럼 NC/Nga 마우스는 약 10주 후 등부위가 비후하거나 외피가 형성되는 것이 확인되었다. 또한 NC/Nga 마우스에서 부전각화증(parakeratosis, 각질세포의 완전 각화가 이루어지지 않고 세포핵이 남아 있는 증상), 각질증식증(hyperkeratosis, 각질층의 비후), 가시세포증(acanthosis, 건선과 같이 표피의 유극세포층의 증식), 단핵구의 세포유출현상(exocytosis, 세포막의 운동에서 필요량 이외의 수분과 세포 분비 물질 등을 세포 밖으로 방출하는 현상) 그리고 표피의 염증세포 침윤 등의 병변이 확인되었다.
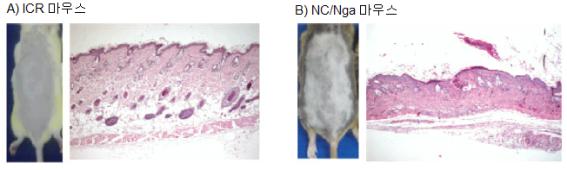
<그림-1> ICR 및 NC/Nga 마우스의 아토피피부염 자연발생모델: ICR 마우스에서는 10주 동안 일반 환경에서 사육 후 어떠한 병변도 나타나지 않았으나 NC/Nga는 육안적 및 조직병리학적 병변이 확인되었다(참고: Pokharel).
2. Hapten-유도 모델
1) 개념
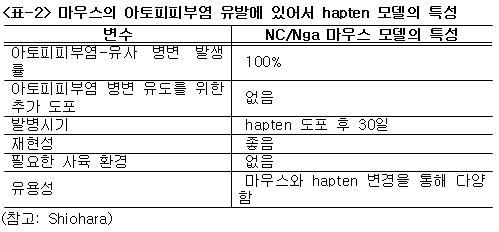
○ 음식 섭취를 통해 면역반응을 유발하는 물질을 음식 알러젠(food allergen)이라고 한다. 대표적인 음식 알러젠은 계란의 ovalbumin과 우유의 casein이 있으며 대부분 수용성 당단백질으로 질량은 10-75 kd이다. 음식 알러젠은 소화에 안정적이기 때문에 원래의 형태로 흡수되어 면역반응을 유발한다. 이들은 항체 IgE와 결합할 수 있는 항원결정기(epitope: 면역 반응을 유발시키는 외부 단백질 혹은 항원의 특정 부위)를 가지고 있기 때문에 면역반응을 유발할 수 있다. 그러나 hapten은 항원결정기가 없기 때문에 그 자체적으로 면역반응을 유발하지 않는다. 따라서 면역반응을 유발하기 위해 hapten은 항원결정기가 있는 단백질과의 결합이 필요하다. 이와 같이 hapten이란 자체적으로는 면역반응을 유발하지 않지만 체내에서 단백질과의 결합을 통해 면역반응을 유발하는 작은 분자의 화학물질을 말한다. 대부분 hapten의 질량은 500 dalton(수소 1개의 질량) 이하이다. 이와 같이 hapten이 체내의 단백질과 결합하는데 이를 단백질을 hapten-운반 adduct(hapten-carrier adduct)라고 한다. 일단 hapten-carrier adduct에 의해 항체가 형성되면 hapten도 IgE 항체에 결합한다. 그러나 때에 따라서는 hapten 자체가 hapten-carrier adduct에 의해 유도된 항체에 결합을 저해하여 hapten-carrier adduct에 의한 면역반응을 막을 수도 있다. 이를 hapten-저해(hapten inhibition)라고 한다. 식이에 포함된 hapten은 마늘의 diallyl disulfide와 탄산음료의 sodium sulphite 등이 있다. 마우스를 이용한 아토피피부염 모델을 위한 가장 많이 이용되는 hapten은 2,4,6-trinitro-1-chrolobenzene(TNCB), 2,4-dinitrochlorobenzene(DNCB), 2,4-dinitrofluorobenzene(DNFB)와 oxazolone이 있으며 TNCB가 가장 대표적이다. 금속이온성 hapten은 Ni 2+ , Co 2+ , Cu 2+ 와 Cr 3+ 이 있으며 사람에서 약 10-15% 정도 피부염을 유발한다. <표-2>는 hapten과 마우스를 이용하여 아토피피부염 모델의 특성을 나타낸 것이다.
2) 방법과 사례
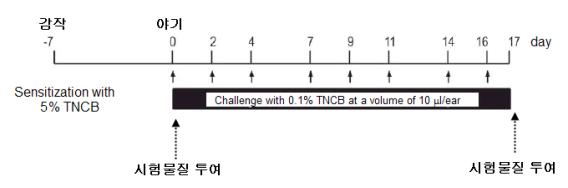
<그림-2> 아토피피부염의 유발과 한약재 시험물질 투여의 예: 단 1회의 높은 농도의 TNCB(trinitrochlorobenzene)을 통한 감작, 낮은 농도 TNCB의 을 여러 번 도포를 통한 야기를 통해 아토피피부염을 가진 마우스 동물모델을 만들 수 있다. 항아토피피부염 약물 개발을 위한 시험물질은 야기 시작 또는 야기 이후에 투여가 이루어진다.
○ 사례: TNCB-BALB/c 모델에 중요한 것은 급성 염증에서 만성염증으로 진행되면서 면역반응의 변화가 유도된다는 것이다. <그림-3>에서처럼 초기 hapten 도포를 통해 Th1세포 활성이 지배적인 환경이 유도되지만 반복적인 hapten 도포를 통해 Th2세포 활성이 지배적인 환경으로 전환된다.
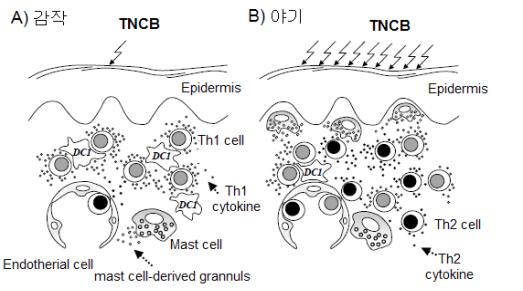
<그림-3> TNCB에 의한 감작과 야기에 따른 면역반응의 변화: BALB/c 마우스에 TNCB(2,4,6-trinitro-1-chrolobenzene) 감작에 의해 Th1세포 및 DC(dentric cell, 수지상세포), 비만세포(mast cell)의 활성이 증가되었지만 반복적인 TNCB 도포에 의해 Th2세포의 활성이 증가된다(참고: Shiohara).
○ 외인성 및 내인성 아토피피부염에서의 면역학적 반응의 차이: 외인성 아토피피부염과 내인성 아토피피부염에서의 면역학적 반응의 차이가 존재한다. 일반적으로 아토피피부염은 외인성 아토피피부염으로 Th2세포 활성의 지배적인 환경이다. 또한 아토피피부염 환자에서 관찰되는 다양한 병리적 반응이 정상적으로 Th2세포 활성을 조율하는 Th1세포 기능의 결함에 기인하는 것으로 이해되고 있다. 그러나 아토피피부염에 있어서 개인별 면역학적 변화가 다양하기 때문에 이에 맞는 치료가 무엇보다도 중요하다. TNCB-BALB/c 모델은 TNCB 및 다른 hapten이나 아토피피부염 유도물질을 이용하여 다양한 면역학적 변화를 유도할 수 있기 때문에 면역학적 개인의 차이를 고려한 약물 개발을 위한 동물모델로 적절할 것으로 고려된다. TNCB-BALB/c 모델은 hapten과 마우스 종을 변경하여 IgE-매개 감각에 의한 외인성 아토피피부염과 IgE-매개 감작이 없는 내인성 아토피피부염 유도에 응용이 가능한 장점이 있다. TNCB-BALB/c 모델은 기본적으로 내인성 특성을 가진 BALB/c 마우스에 TNCB의 반복적인 노출을 통해 Th2세포 활성의 유도를 위해 개발되었다. 그러나 TNCB에 의해 감작된 BALB/c 마우스에서 hapten인 oxazolone 도포는 급성병변에서 Th1세포와 Th2세포의 활성이 공존하는 특성을 유도한다. 그러나 지속적인 oxazolone 도포에 의한 만성병변에서는 Th2세포 활성의 지배적인 환경이 유도된다. 또한 oxazolone을 C57BL/6 마우스에 노출하면 IgE 혈청농도 증가나 즉시형 면역반응이 없이 Th2세포-지배적인 만성염증반응이 유발된다. 일반적으로 TNCB는 BALB/c 마우스를 이용하여 외인성 아토피피부염을 유도하는데 적절한 hapten이며 oxazolone은 C57BL/6 마우스를 이용하여 내인성 아토피피부염을 유도하는데 적절한 것으로 평가되고 있다. 따라서 아토피피부염의 개인별 면역학적 차이를 반영한 한약재 치료약물의 개발을 위해서는 마우스의 종과 hapten의 종류를 다르게 하여 적절한 모델로 개발, 응용할 수 있다. TNCB-BALB/c 모델에서 아토피피부염 병변을 유발하는데 소요되는 시간은 30일 정도로 비교적 짧다는 장점이 있다. 반면에 감작과 야기가 화학물질이기 때문에 이들의 활성에 의해 치료약물과 혼합될 우려가 있다는 것이 단점이다. 아토피피부염에 대한 약물개발의 목적으로 이 모델을 이용하기 위해서는 2가지 측면에서 한약재의 투여시기를 고려할 수 있다. 예방차원에서의 한약재 개발이라면 감작 후 야기를 위한 반복적인 도포와 더불어 한약재 투여를 시작할 수 있다. 또한 치료목적의 차원에서는 야기가 끝난 한약재 투여를 시작할 수 있다.
3. Tape-stripping/epicutaneous OVA sensitization
1) 개념
○ 마우스에 단백질 항원인 ovalbumin(OVA)을 피부손상과 관계없이 테이프에 흡착하여 아토피피부염-유사 병변을 유발하는 모델을 Tape-stripping/epicutaneous OVA sensitization model(테이프-오발부민 감작 모델, OVA-감작 모델)이라고 한다. OVA-감작 모델은 BALB/c와 C57BL/6 마우스를 이용하여 Th2세포 활성의 지배적인 환경을 유도한다. 마우스의 등쪽 피부의 털을 밀어내고 테이프로 약 6번 정도 접착-분리를 반복한다. 접착-분리를 반복하면 아토피피부염의 환자에서 긁어서 형성된 피부상처와 같이 유사한 병변이 형성된다. 이러한 반복적인 접착-분리는 피부장벽 손상을 통한 단백질 항원의 피내 침투이기 때문에 OVA-감작 모델이 외인성 아토피피부염을 유발하는데 응용될 수 있다.
2) 방법
○ <그림-4>에서처럼 식염수 100 μl에 100 μg ovalbumin을 용해시킨 용액을 멸균거즈(sterile gauze)의 1x1 cm 패치에 적용하여 감작을 유도한다. 이때 투명 드레싱을 이용하여 항원이 빠져 나오는 것을 막는다. 약 1주일 후 패치를 제거하고 2주 후에 다시 동일한 패치를 동일한 피부 부위에 적용하는 감작을 총 3번 한다. 피내 감작된 마우스 피부에서 긁는 횟수의 증가, 표피와 진피의 두께 증가, T-세포와 호산구의 침윤, Th2세포 사이토카인인 IL-4, IL-5, IL-13과 케모킨이 증가하는 면역학적 변화가 유도된다.
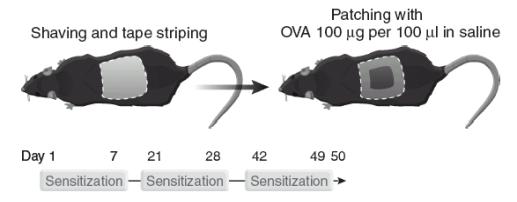
<그림-4> Tape-stripping/epicutaneous OVA sensitization: 식염수 100 μl에 100 μg ovalbumin을 용해시킨 용액을 멸균거즈(sterile gauze)의 1x1 cm 패치에 적용하여 감작을 유도한다. 약 1주일 후 패치를 제거하고 약 2주 후에 다시 동일한 패치를 동일한 피부 부위에 적용하는 감작을 총 3번 한다(참고: Jin).
4. 집먼지 진드기-페치(patch) 모델
○ 집먼지 진드기 항원이 부착된 페치를 피부에 접촉하는 페치테스트를 통해 아토피피부염을 가진 환자에게 높은 양성반응이 확인할 수 있다. 이는 집먼지 진드기도 아토피피부염의 주요 원인물질로 작용한다는 것을 의미한다. 집먼지 진드기(house dust mite) 모델은 Dermatophagoides pteronyssinus 또는 Dermatophagoides farinae 로부터 얻은 추출물을 페치 형태로 마우스 피부에 접착하여 아토피피부염-유사 병변을 유발하는 모델이다. BALB/c 마우스에 집먼지 진드기의 추출물을 피내 감작한 결과, 표피의 이상증식(hyperplasia)과 해면화(spongiosis)를 비롯하여 T-세포의 침윤이 확인되었다. 특히 Th2세포의 지배적 환경이 국소적 또는 전신적으로 나타났다. 대체적으로 집먼지 진드기의 추출물에 의한 아토피피부염-유사 증상 및 병변은 obalbumin 감작에 나타나는 것과 유사한 것으로 알려졌다.
5. 유전자-조작 모델
○ 유전자-조작 모델이란 특정 유전자를 제거(knockout)하거나 형질전환(transgenic)하여 아토피피부염-유사 병변을 유도하는 모델이다. 그러나 대부분의 유전자-조작 모델은 아토피피부염의 일부 현상만 유도하기 때문에 아토피피부염의 전체적인 증상을 유도하지 못하는 단점이 있다. 아토피피부염을 위한 형질전환 모델에 있어서 제거되는 대표적인 유전자은 IL-4 유전자이다. IL-4는 Th2세포의 활성화와 IgE 생성에 있어서 중심적인 역할을 하는 사이토카인이다. IL-4 유전자의 형질전환된 마우스에서 소양증, 가피, 태선화의 병변과 습진을 유도하는 면역병리학적 변화가 확인되었다.